1. Основни знания (ако искате да видите експерименталната част, моля, прехвърлете директно към втората част)
Като производна реакция на конвенционалната PCR, PCR в реално време основно следи промяната на количеството продукт на амплификация във всеки цикъл на реакцията на амплификация на PCR в реално време чрез промяна на флуоресцентния сигнал и количествено анализира началния шаблон чрез връзката между стойността на ct и стандартната крива.
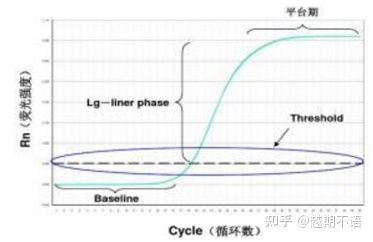
Специфичните данни на RT-PCR сабазова линия, праг на флуоресценцияиCt стойност.
| базова линия: | Стойността на флуоресценцията на 3-ия-15-ия цикъл е базовата линия (базова линия), която се причинява от случайна грешка на измерването. |
| Праг (праг): | Отнася се за границата на откриване на флуоресценция, зададена на подходяща позиция в областта на експоненциален растеж на кривата на усилване, обикновено 10 пъти стандартното отклонение от базовата линия. |
| CT стойност: | Това е броят на PCR циклите, когато стойността на флуоресценция във всяка реакционна епруветка достигне прага. Стойността на Ct е обратно пропорционална на количеството на първоначалния шаблон. |
Общи методи за етикетиране за RT-PCR:
| метод | предимство | недостатък | обхват на приложение |
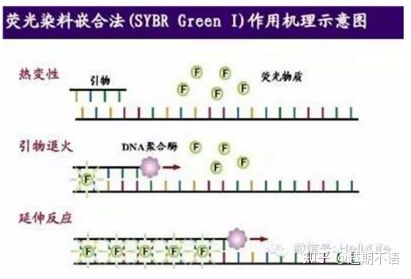
| SYBR GreenⅠ | Широка приложимост, чувствителен, евтин и удобен | Изискванията за праймер са високи, склонни към неспецифични ленти | Подходящ е за количествен анализ на различни целеви гени, изследване на генна експресия и изследване на трансгенни рекомбинантни животни и растения. |
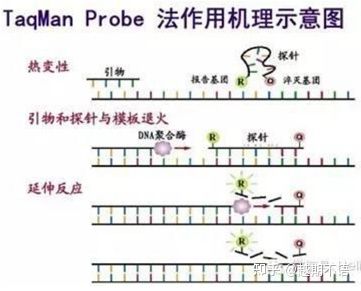
| TaqMan | Добра специфичност и висока повторяемост | Цената е висока и е подходяща само за конкретни цели. | Откриване на патогени, изследване на гени за лекарствена резистентност, оценка на ефикасността на лекарствата, диагностика на генетични заболявания. |
| молекулярен маяк | Висока специфичност, флуоресценция, нисък фон | Цената е висока, подходяща е само за конкретна цел, дизайнът е труден и цената е висока. | Специфичен генен анализ, SNP анализ |
2. Експериментални стъпки
2.1 За експерименталното групиране- трябва да има множество кладенци в групата и трябва да има биологични повторения.
| ① | Празен контрол | Използва се за откриване на състоянието на клетъчния растеж при експерименти |
| ② | Отрицателна контрола siRNA (неспецифична siRNA последователност) | Демонстрирайте спецификата на действието на RNAi.siRNA може да индуцира неспецифичен отговор на стрес при концентрация от 200 nM. |
| ③ | Контролен реагент за трансфекция | Изключете токсичността на трансфекционния реагент към клетките или ефекта върху експресията на целевия ген |
| ④ | siRNA срещу целеви ген | Намалете експресията на целевия ген |
| ⑤ (по избор) | положителна siRNA | Използва се за отстраняване на проблеми с експериментална система и оперативни проблеми |
| ⑥ (по избор) | Флуоресцентна контролна siRNA | Ефективността на клетъчната трансфекция може да се наблюдава с микроскоп |
2.2 Принципи на проектиране на грундове
| Увеличен размер на фрагмента | За предпочитане при 100-150 bp |
| Дължина на грунд | 18-25 bp |
| GC съдържание | 30%-70%, за предпочитане 45%-55% |
| Tm стойност | 58-60 ℃ |
| Последователност | Избягвайте непрекъснато T/C;A/G непрекъснато |
| 3 крайна последователност | Избягвайте GC rich или AT rich;крайната основа за предпочитане е G или C;най-добре е да избягвате Т |
| Допълване | Избягвайте комплементарни последователности от повече от 3 бази в праймера или между два праймера |
| Специфичност | Използвайте blast search, за да потвърдите специфичността на праймера |
①SiRNA е специфична за видовете и последователностите на различните видове ще бъдат различни.
②SiRNA е опакована в лиофилизиран прах, който може да се съхранява стабилно 2-4 седмици при стайна температура.
2.3 Инструменти или реактиви, които трябва да се подготвят предварително
| Буквар (вътрешна справка) | Включително два напред и назад |
| Праймери (целеви ген) | Включително два напред и назад |
| Целева Si РНК (3 ленти) | Обикновено компанията ще синтезира 3 ленти и след това ще избере една от трите чрез RT-PCR |
| Комплект за трансфекция | Lipo2000 и др. |
| Комплект за бързо извличане на РНК | За екстракция на РНК след трансфекция |
| Комплект за бърза обратна транскрипция | за cDNA синтез |
| Комплект за PCR амплификация | 2×Super SYBR Green qPCR Master Mix |
2.4 По отношение на проблемите, на които трябва да се обърне внимание в конкретните експериментални стъпки:
①процес на трансфекция на siRNA
1. За посяване можете да изберете 24-ямкова плака, 12-ямкова плака или 6-ямкова плака (средната концентрация на РНК, предложена във всяка ямка на 24-ямкова плака е около 100-300 ng/uL), а оптималната плътност на трансфекция на клетките е до 60%-80% или така
2. Стъпките на трансфекция и специфичните изисквания са стриктно в съответствие с инструкциите.
3. След трансфекция, пробите могат да бъдат събрани в рамките на 24-72 часа за откриване на иРНК (RT-PCR) или откриване на протеин в рамките на 48-96 часа (WB)
② процес на екстракция на РНК
1. Предотвратяване на замърсяване от екзогенни ензими.Основно включва стриктно носене на маски и ръкавици;използване на стерилизирани накрайници за пипети и ЕР тръби;водата, използвана в експеримента, трябва да бъде свободна от РНКаза.
2. Препоръчително е да направите два пъти, както е предложено в комплекта за бързо извличане, което наистина ще подобри чистотата и добива.
3. Отпадъчната течност не трябва да докосва РНК колоната.
③ Количествено определяне на РНК
След като РНК бъде извлечена, тя може да бъде количествено определена директно с Nanodrop и минималното отчитане може да бъде толкова ниско, колкото 10 ng/ul.
④Процес на обратна транскрипция
1. Поради високата чувствителност на RT-qPCR трябва да се направят поне 3 паралелни ямки за всяка проба, за да се предотврати последващото Ct да бъде твърде различно или SD да бъде твърде голямо за статистически анализ.
2. Не замразявайте и размразявайте Master mix многократно.
3. Всяка тръба/отвор трябва да се смени с нов накрайник!Не използвайте непрекъснато един и същ връх на пипетата за добавяне на проби!
4. Филмът, прикрепен към 96-ямковата плака след добавяне на пробата, трябва да се изглади с плака.Най-добре е да се центрофугира, преди да се постави в машината, така че течността по стената на тръбата да може да потече надолу и да премахне въздушните мехурчета.
⑤Общ анализ на кривата
| Няма период на логаритмичен растеж | Вероятна висока концентрация на шаблон |
| Няма CT стойност | Неправилни стъпки за откриване на флуоресцентни сигнали; разграждане на праймери или сонди – неговата цялост може да бъде открита чрез PAGE електрофореза; недостатъчно количество шаблон; разграждане на шаблоните – избягване на въвеждането на примеси и многократно замразяване и размразяване при подготовката на пробите; |
| Ct>38 | Ниска ефективност на усилване;PCR продуктът е твърде дълъг;различни компоненти на реакцията се разграждат |
| Линейна крива на усилване | Сондите могат да бъдат частично разградени от повтарящи се цикли на замразяване-размразяване или продължително излагане на светлина |
| Разликата в дублиращите дупки е особено голяма | Реакционният разтвор не е напълно разтопен или реакционният разтвор не е смесен;термичната баня на PCR инструмента е замърсена с флуоресцентни вещества |
2.5 Относно анализа на данни
Анализът на данните от qPCR може да бъде разделен на относително количествено определяне и абсолютно количествено определяне.Например клетките в групата на лечение в сравнение с клетките в контролната група,
Колко пъти се променя иРНК на гена X, това е относително количествено определяне;в определен брой клетки иРНК на X гена
Колко копия има, това е абсолютно количествено изражение.Обикновено това, което използваме най-много в лабораторията, е относителният количествен метод.обикновено,методът 2-ΔΔctсе използва най-много в експерименти, така че само този метод ще бъде представен подробно тук.
2-ΔΔct метод: Полученият резултат е разликата в експресията на целевия ген в експерименталната група спрямо целевия ген в контролната група.Изисква се ефективността на амплификация както на целевия ген, така и на вътрешния референтен ген да са близки до 100%, а относителното отклонение не трябва да надвишава 5%.
Методът на изчисление е следният:
Δct контролна група = ct стойност на целевия ген в контролната група – ct стойност на вътрешния референтен ген в контролната група
Δct експериментална група = ct стойност на целевия ген в експерименталната група – ct стойност на вътрешния референтен ген в експерименталната група
ΔΔct=Δct експериментална група-Δct контролна група
И накрая, изчислете кратното на разликата в нивото на изразяване:
Change Fold=2-ΔΔct (съответстващо на функцията на excel е POWER)
Свързани продукти:
Време на публикуване: 20 май 2023 г