Преглед
Бърза идентификация на трансгенни растения
Текст/Tong Yucheng
Експериментална операция/Han Ying
Редактор/Уен Юджун
Думи/1600+
Препоръчително време за четене/8-10 минути
Бърза идентификация на трансгенни растения
Като новодошъл в лабораторията не е добра работа да отсявате положителни растения от куп растения с нисък процент на преобразуване.Първо трябва да се извлече ДНК от голям брой проби една по една и след това чуждите гени ще бъдат открити чрез PCR.Резултатите обаче често са празни и понякога са ленти с няколко елемента, но е невъзможно да се определи дали има пропуснати откривания или фалшиви откривания..Много ли е безпомощно да се изправиш срещу такъв експериментален процес и резултати?Не се тревожи, брат те учи как лесно и точно да отсяваш трансгенни положителни растения.
Етап 1: Праймери за откриване на дизайн
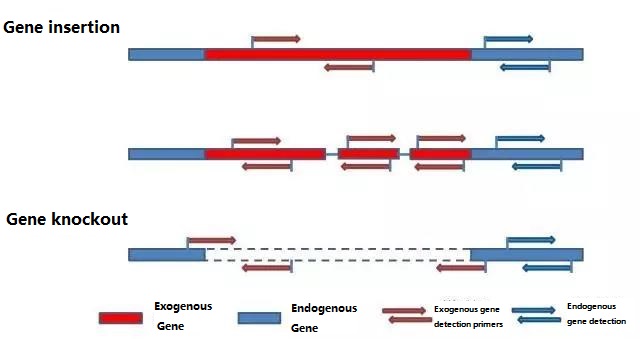
Определете ендогенния ген и екзогенния ген, които да бъдат открити според пробата, която ще се тества, и изберете представителна последователност от 100-500 bp в гена за проектиране на праймера.Добрите праймери могат да гарантират точността на резултатите от откриването и да съкратят времето за откриване (вижте приложението за често използвани праймери за откриване).
Забележка:
Новопроектираните праймери трябва да оптимизират условията на реакция и да проверят точността, прецизността и границата на откриване на откриването, преди да извършат широкомащабно откриване.
Стъпка 2:Разработване на експериментален протокол

Положителна контрола: Използвайте пречистената ДНК, съдържаща целевия фрагмент, като шаблон, за да определите дали PCR реакционната система и условията са нормални.
Отрицателна/празна контрола: Използвайте ДНК шаблон или ddH2O, който не съдържа целевия фрагмент като шаблон за откриване дали има източник на замърсяване в PCR системата.
Вътрешен референтен контрол: използвайте комбинацията праймер/сонда на ендогенния ген на пробата, която ще се тества, за да прецените дали шаблонът може да бъде открит чрез PCR.
Забележка:
За всеки тест трябва да се зададат положителни, отрицателни/празни контроли и вътрешни контроли, за да се оцени валидността на експерименталните резултати.
Стъпка 3: Подготовка на експеримента

Преди употреба проверете дали разтворът е смесен равномерно.Ако се установи утайка, тя трябва да се разтвори и разбърка според инструкциите преди употреба.2×PCR смес трябва да се пипетира и смеси многократно с микропипета преди употреба, за да се избегне неравномерно разпределение на йони.
Забележка:
Извадете инструкциите и ги прочетете внимателно и направете подготовка преди експеримента в строго съответствие с инструкциите.
Стъпка 4: Подгответе PCR реакционна система
Съгласно експерименталния протокол, смесете праймерите, H2O, 2 × PCR смесете, центрофугирайте и ги разпределете във всяка реакционна епруветка.
Забележка:
За широкомащабно или дългосрочно тестване се препоръчва използването на PCR реакционна система, съдържаща UNG ензим, който може ефективно да избегне аерозолно замърсяване, причинено от PCR продукти.
Стъпка 5: Добавете шаблон за реакция

Използвайки технологията Direct PCR, няма нужда от досаден процес на пречистване на нуклеинова киселина.Шаблонът на пробата може да бъде приготвен в рамките на 10 минути и добавен към съответната PCR реакционна система.
Забележка:
Методът на лизис има по-добър ефект на откриване и полученият продукт може да се използва за множество реакции на откриване.
5.1: Директен PCR на листа
Според размера на картинката в ръководството, изрежете листната тъкан с диаметър 2-3 mm и я поставете в PCR реакционната система.
Забележка: Уверете се, че листните фрагменти са напълно потопени в PCR реакционния разтвор и не добавяйте прекалено много листна тъкан.
5.2: Метод на лизис на листа
Нарежете листната тъкан с диаметър 5-7 mm и я поставете в центрофужна епруветка.Ако изберете зрели листа, моля, избягвайте да използвате тъканите на главната жилка на листа.Пипетирайте 50 ul буфер P1 лизат в центрофужна епруветка, за да се уверите, че лизатът може напълно да потопи листната тъкан, поставете го в термоциклер или метална баня и лизирайте при 95°C за 5-10 минути.


Добавете 50 ul буфер P2 неутрализиращ разтвор и разбъркайте добре.Полученият лизат може да се използва като шаблон и да се добави към PCR реакционната система.
Забележка: Количеството на шаблона трябва да бъде между 5-10% от PCR системата и не трябва да надвишава 20% (например, в 20 μl PCR система, добавете 1-2 μl лизисен буфер, не повече от 4 μl).
Стъпка 6: PCR реакция

След центрофугиране на епруветката за PCR реакция, поставете ги в PCR инструмент за амплификация.
Забележка:
Реакцията използва непречистена матрица за амплификация, така че броят на циклите на амплификация е с 5-10 повече цикъла, отколкото при използване на пречистена ДНК матрица.
Стъпка 7: Откриване на електрофореза и анализ на резултатите

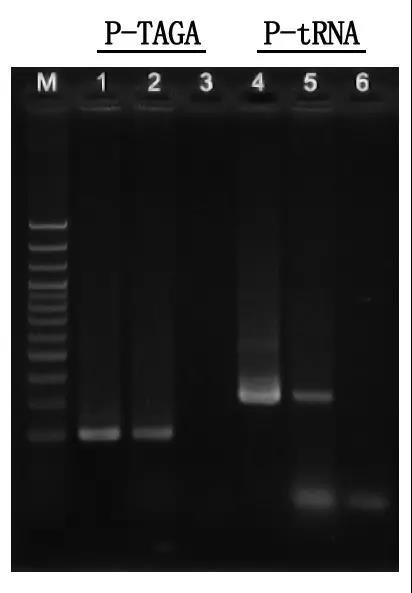
M: 100bp ДНК стълба
1\4: Метод на пречистена ДНК
2\5: Директен PCR метод
3\6: Празна контрола
Контрол на качеството:
Резултатите от теста на различните контроли, зададени в експеримента, трябва да отговарят на следните условия.В противен случай трябва да се анализира причината за проблема и тестът да се извърши отново, след като проблемът бъде отстранен.
Таблица 1. Нормални резултати от тестове на различни контролни групи

*Когато плазмидът се използва като положителна контрола, резултатът от ендогенния генен тест може да бъде отрицателен
Преценка на резултата:
A. Резултатът от теста на ендогенния ген на пробата е отрицателен, което показва, че ДНК, подходяща за обикновена PCR детекция, не може да бъде извлечена от пробата или извлечената ДНК съдържа инхибитори на PCR реакцията и ДНК трябва да бъде извлечена отново.
B. Резултатът от теста на ендогенния ген на пробата е положителен, а резултатът от теста на екзогенния ген е отрицателен, което показва, че ДНК, подходяща за обикновена PCR детекция, е извлечена от пробата и може да се прецени, че XXX генът не е открит в пробата.
C. Резултатът от теста на ендогенния ген на пробата е положителен, а резултатът от теста на екзогенния ген е положителен, което показва, че ДНК, подходяща за обикновена PCR детекция, е извлечена от пробата и ДНК на пробата съдържа XXX гена.Експериментите за потвърждение могат да бъдат допълнително проведени.
Стъпка 8: Праймери за откриване на дизайн

След експеримента използвайте 2% разтвор на натриев хипохлорит и 70% разтвор на етанол, за да избършете експерименталната зона, за да предотвратите замърсяване на околната среда.
Приложение
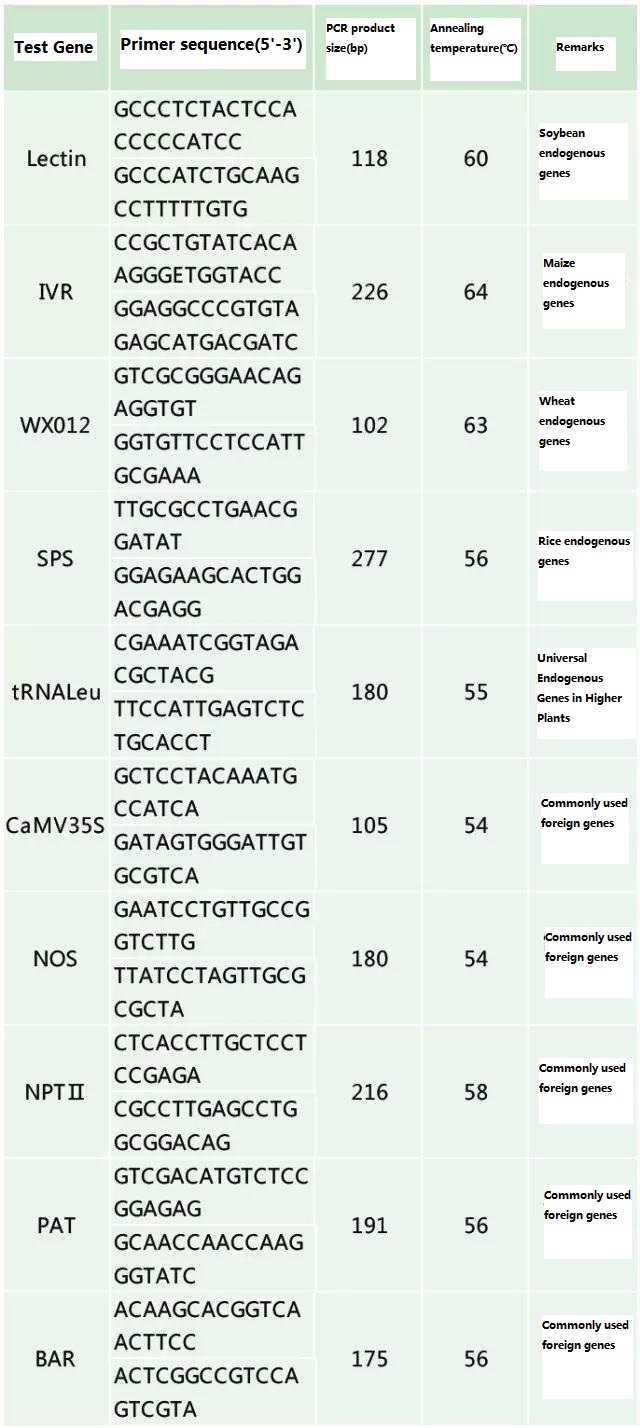
Таблица 2. Често използвани праймери за обща PCR детекция на генетично модифицирани растения
Референтен документ:
SN/T 1202-2010, Метод за качествен PCR откриване на генетично модифицирани растителни съставки в храната.
Съобщение на Министерството на земеделието 1485-5-2010, Тестване на съставките на генетично модифицирани растения и техните продукти - ориз M12 и неговите производни.
Време на публикуване: 09 юни 2021 г








